Wasser ist (nicht nur) zum Waschen da!
Lösungen für fotografische Zwecke
Man nehme...
Die Hauptzutat fotografischer Lösungen
ist - richtig:
Wasser
In den meisten Fällen reicht
normales Leitungswasser, Trinkwasser, aus, da dieses in Deutschland von recht
hoher, gesetzlich geregelter Qualität ist. Aber: auch Stoffe, die im Trinkwasser
zugelassen sind, weil sie gesundheitlich unbedenklich sind, z.B. Kalzium- und
Magnesiumsalze, können die im Zuge der Verarbeitung ablaufenden chemischen
Reaktionen beeinflussen. Die Hersteller fotografischer Lösungen versuchen
durch Hilfsstoffe z.B. die Wasserhärte - eben jene Kalzium- und Magnesiumsalze
- zu maskieren, so dass sie die Verarbeitung nicht stören. So lange die
Zusammensetzung des Wassers konstant ist, ist auch die durch Beimengungen verursachte
Beeinflussung konstant und stört nicht, wenn man seine Verarbeitung selbst
kalibriert hat. Störend sind Prozessschwankungen durch Änderungen
der Wasserqualität, weil man bei der Aufnahme dann nie weiß, was
bei der Verarbeitung mit dem Bild passieren wird.
Folgende Empfehlungen sollte man beherzigen, wenn man auf der sicheren Seite
liegen möchte:
• Leitungswasser
für Fixierbäder
• Schwebstofffreies Wasser für die meisten alkalischen Entwickler
und Abschwächerlösungen
• Demineralisiertes Wasser für Feinkornentwickler und Verstärkerlösungen
sowie auf jeden Fall für Toner
Wenn das vorhandene Leitungswasser extrem hart ist (Auskunft dazu können
die lokalen Wasserwerke geben.) und demineralisiertes Wasser nicht verfügbar
ist, kann man sich helfen, indem man Leitungswasser für 20 Minuten kochen
lässt. Das fällt praktisch die gesamte Wasserhärte in Form unlöslicher
Niederschläge aus und treibt alle gelösten Gase aus.
Filtern nach dem Abkühlen entfernt die ausgefällten Niederschläge.
(Man sollte allerdings nur im Notfall zu dieser Lösung greifen, da die
Kocherei ziemlich viel Energie verschlingt und das so gereinigte Wasser teuer
und wenig umweltfreundlich macht. Lange dauern tut´s auch: 20 min Kochen
plus ein Vielfaches davon, bis das Wasser so kühl ist, dass man es zum
Ansatz verwenden kann.)
Konzentration ist alles
Die Stärke einer Lösung ist ihre Konzentration oder auch Verdünnung.
Am verbreitetsten sind
Konzentrationsangaben in Teilen
Beispiele sind etwa Entwicklerverdünnungen wie 1+4 oder 1:4. Dabei sind
die beiden Angaben nicht gleichwertig:
1+4 bedeutet, dass sich die Gesamtmenge aus 5 Teilen zusammensetzt, nämlich
1 Teil Konzentrat plus 4 Teile Wasser.
1:4 bedeutet, dass die Gesamtmenge aus 4 Teilen besteht, von denen 1 Teil Konzentrat
ist.
Man sieht schnell, dass die beiden Angaben umrechenbar sind: 1+4 ist gleichwertig
mit 1:5.
Bei großen Gesamtmengen, z.B. einem Ansatz von 1+100, ist der Unterschied
natürlich marginal.
Konzentrationen in Prozent
Wenn die Rede ist von einer 2%igen Natriumsulfitlösung (z.B. als bewährte
Wässerungshilfe), ist die Frage, "2% von was?". Solche Lösungen
sind ein typisches Beispiel für den Vergleich von Äpfeln mit Birnen.
Gemeint ist nämlich: Man nehme 20 g (also eine bestimmte Masse) Natriumsulfit,
löse diese in Wasser auf, das man dann auf 1 l (also ein bestimmtes Volumen)
auffüllt. Die Angabe sind also "Prozent Gewicht je Endvolumen"
(engl.: % w/v für weight/volume).
Entsprechend ist es überraschenderweise möglich, mehr als 100%ige
Lösungen zu erzeugen, wenn die gelöste Substanz sehr gut löslich
ist. Man kann z.B. eine 100%ige Natriumthiosulfatlösung bereiten, indem
man 100 g Natriumthiosulfat in Wasser auflöst und auf 100 ml verdünnt.
Wenn man von einer vorhandenen konzentrierten Lösung ausgeht, die verdünnt
werden soll, ist es gebräuchlich, Volumenprozent (engl.: % v/v für
volume/volume) als Konzentrationsangabe zu benutzen: Für eine 10%ige Lösung
einer Flüssigkeit A nehme man 10 ml von A und verdünne auf 100 ml
Lösung.
Beispiel: Eine 2%ige Essigsäure bekomme ich, wenn ich 2 ml Eisessig (konz.
Essigsäure) auf 100 ml Lösung auffülle. (Tatsächlich enthält
Eisessig aber rund ein halbes Prozent Wasser, so dass die Lösung nicht
genau 2%ig ist, aber für alle praktischen Zwecke ist die Angabe genau genug.)
Die Krise bekommen viele Laboranten, wenn von ihnen z.B. verlangt wird, aus
28%iger Essigsäure (die viel weniger gefährlich in der Handhabung
ist als Eisessig), eine 10%ige Lösung anzusetzen. Hier hilft die
Kreuzmischregel
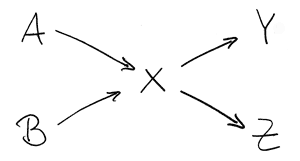
Dabei ist:
A die prozentuale Konzentration der zu verdünnenden Lösung
B prozentuale Konzentration der zum Verdünnen verwendeten Lösung (bei
Wasser B = 0)
X prozentuale Konzentration der gewünschten Lösung
Y = X-B das zu verwendende Volumen der zu verdünnenden Lösung
Z = A-X das zu verwendende Volumen des "Verdünnungsmittels"
Klartext: Y ml Lösung der prozentualen Konzentration A plus Z ml Lösung
der prozentualen Stärke B ergeben eine Lösung der gewünschten
prozentualen Konzentration X.
Beispiel: Die genannte 28%ige Essigsäure soll mit Wasser auf 10%
verdünnt werden.
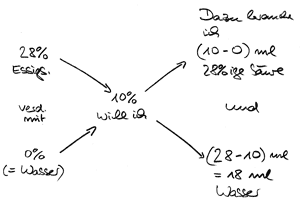
Also geben 10 ml 28%iger Essigsäure plus 18 ml Wasser eine 10%ige Essigsäure.
Wasser und Säure - da wird es bei einigen klingeln. Da war doch dieser
Spruch im Chemieunterricht:
"Gießt du Wasser auf die Säure, dann geschieht das Ungeheure!"
Der Reim klingt harmloser als er ist: Bei der Mischung von Wasser und Säure
wird durch eine chemische Reaktion Energie frei, die dazu führt, dass sich
die Mischung erwärmt. Ist die Säure sehr konzentriert und kommt nur
wenig Wasser dazu, so wird auf engem Raum sehr schnell sehr viel Energie frei
gesetzt. Die Folge ist, dass sich an dieser Stelle die Mischung plötzlich
so weit erhitzt, dass das Wasser schlagartig verdampfen kann. Dann spritzt es
möglicherweise, und was da spritzt ist nicht nur Wasser, sondern auch die
konzentrierte Säure.
Die Situation ist entschärft, wenn man Säure auf Wasser gießt.
Warum? Es ist viel Wasser da, in dem sich die Säuremoleküle und die
entstehende Wärme gut verteilen können. Man gießt also ein wenig
Säure langsam in viel Wasser. Dann passiert nichts Schlimmes.
Der Spruch gilt übrigens in gleicher Weise für starke Basen: Auch
bei der Zugabe von Wasser z.B. zu Natriumhydroxid kann es zu explosionsartigem
Sieden des Wassers kommen. Verlust des Augenlichts und Verätzungen (teilweise
mit bleibenden Vernarbungen) können die Folgen solcher Achtlosigkeit sein.
Das Thema
Sicherheit im privaten Umfeld
ist überhaupt ein trauriges. Im beruflichen Umfeld ist durch arbeitsrechtliche
Vorschriften in aller Regel gut für die Sicherheit von Arbeitnehmern gesorgt,
doch daheim sieht es anders aus: Nicht nur, dass es keinen Sicherheitsingenieur
gibt, der auf die Einhaltung der Sicherheitsvorgaben achtet. Zu allem Überfluss
sind es oft auch noch unzureichend ausgebildete Leute, die mit den gefährlichsten
Substanzen hantieren. Der am Arbeitsplatz durch Vorschriften und ggf. Aufpasser
gut beschützte Chemielaborant hat im Rahmen seiner Ausbildung gelernt,
mit Gefahrstoffen umzugehen, der nicht geschulte "Künstler" in
der Dunkelkammer aber nicht. So wundert es nicht, dass daheim viele, teilweise
fatale, Unfälle passieren.
Um das Ganze abzurunden, finden es viele Leute auch noch ausgesprochen "cool",
sich wissentlich Gefahren auszusetzen. Sind doch alles Memmen, die beim Hantieren
mit Chemikalien Handschuhe und Schutzbrille tragen oder ihre Finger nicht in
den Entwickler, möglichst Pyro, tauchen wollen. Wer derart spätpubertär
anmutende Äußerungen von sich gibt, kann mir nur leid tun.
Wenn Sie nicht wissen, welche Gefahren ein Stoff birgt,
behandeln Sie ihn in Ihrem eigenen Interesse mit Respekt!
Zwar werden die Bilder der meisten Künstler erst nach dem Tod der Künstler
richtig wertvoll, aber die Künstler haben dann nichts mehr davon, und die
Nachkommen hätten vielleicht auch mehr von Vater oder Mutter als vom Geld
für deren Bilder.
(Nachtrag: Meine Frau meint, ich solle Ihnen nicht gleich Ihr baldiges Ableben
in Aussicht stellen. So dramatisch sei es doch vielleicht nicht. Sie hat Recht:
Sie werden nicht morgen sterben, wenn Sie heute Ihre Finger Hydrochinon oder
Pyrogallol enthaltende Entwickler tauchen. Allerdings steigen Ihre Chancen auf
gesundheitliche Spätfolgen dramatisch an. Insofern bitte ich Sie, mir meinen
Hang zum Zynismus nachzusehen.)
Verschiedene Formen einer Substanz
Manche Fotochemikalien kommen in verschiedenen Formen vor. Beispiele sind Soda
sicc., Soda-Monohydrat und Soda krist. (Dekahydrat). Der Unterschied ist hier
der Wassergehalt: Soda sicc. ist die wasserfreie Form und enthält kein
Kristallwasser. Soda-Monohydrat enthält je Sodamolekül ein Wassermolekül
und Soda krist. (Kristallsoda oder Dekahydrat) je Sodamolekül 10 Wassermoleküle.
Wenn ich also von jedem dieser drei Stoffe 10 g auf der Waage habe, habe ich
nur im ersten Fall 10 g Wirksubstanz, bei den Formen mit Kristallwasser um so
weniger, je mehr Wasser enthalten ist. Für einige häufig vorkommende
Substanzen ist in der nachfolgenden Tabelle aufgelistet, wie man die Mengen
umrechnen muss, wenn man die eine durch die andere ersetzt.
| Substanz |
Diese
Menge wasserfreie Form ist zu ersetzen durch |
diese
Menge Gramm des Monohydrats |
oder
diese Menge der kristallinen Form
(in Klammern Anzahl der Wassermoleküle) |
Soda
(Natriumkarbonat) |
1 |
1,17 |
2,7
(10) |
| Natriumsulfit |
1 |
|
2
(7) |
| Natriumsulfat |
1 |
|
2,3
(10) |
| Natriumthiosulfat |
1 |
|
1,6
(5) |
Die
kristallinen Formen, inbesondere von Natriumthiosulfat, das sehr gut in Wasser
löslich ist, können interessante Wirkungen haben: Löst man sie
in Wasser auf, so kühlt sich die Lösung stark ab. Dieser Abkühlungsvorgang
kann beim Auflösen größerer Mengen so weit gehen, dass die Lösung
gefriert und den Behälter, in dem man mischt, zum Platzen bringt. Es empfiehlt
sich also, auch um Zeit zu sparen, zum Ansatz warmes Wasser zu verwenden, denn
in kaltem Wasser lösen sich Kristalle nur sehr langsam.
Bei Auflösen der wasserfreien Formen in Wasser dagegen wird Wärme
frei (vgl. Wasser auf Säure), und hier empfiehlt es sich folgerichtig,
kaltes Wasser zu verwenden und immer die Wirksubstanz zum Wasser zu geben und
nicht umgekehrt.
Temperaturumrechnung
In der Schule hat man Sie im Physikunterricht sicher mit der Kelvinskala gequält,
und die meisten wissen, dass man von einer Temperatur in Kelvin (nicht: Grad
Kelvin! Abgekürzt nur mit K, nicht °K) nur 273 (genauer 273,15)
abziehen muss, um die Temperatur in Grad Celsius (°C) zu erhalten. Kelvin
in Grad Celsius ist leicht umzurechnen, aber in der Fotografie leider unüblich.
Häufig kommt dagegen das in den USA noch immer übliche Grad Fahrenheit
(°F) vor. Auf der Fahrenheit-Skala gefriert Wasser bei 32°F und kocht
bei 212°F. Damit ist eigentlich alles gesagt.
Na gut, sagen wir es konkreter:
Um von °F in °C umzurechnen, subtrahieren Sie 32 und teilen Sie
durch 1,8.
Um von °C in °F umzurechnen, multiplizieren Sie mit 1,8 und addieren
Sie 32.
Damit ist klar: Die Standardtemperatur fotografischer Lösungen von 20°C
wird auf der anderen Seite des großen Teiches 68°F betragen, ohne
deswegen wärmer zu sein.
Literatur
Die meisten dieser Zusammenhänge sind zusammengestellt in:
Grant Haist, Modern Photographic Processing, Vol. 1, Wiley Interscience
(Wiley Series on photographic sciences and technology), 1979, ISBN 0-471-02228-4
[m.W. leider lange vergriffen und nur noch in Antiquariaten zu haben]

